장기적 추적 조사 및 모든 비용 코오롱 부담
약사법 개정 통해 업체 허위자료 처벌 강화
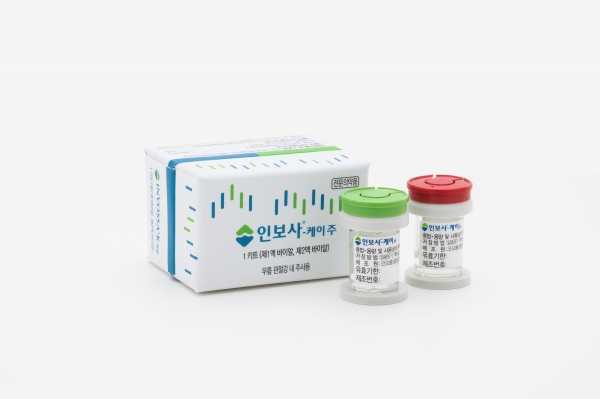
[스트레이트뉴스=윤대우 기자] 식품의약품안전처가 골관절염 유전자치료제 인보사케이주(인보사)사태와 관련 주무감독 기관으로 허가 및 관리소홀 미흡 등 책임을 다하지 못한 것에 대해 대국민 사과를 했다.
이의경 식약처장은 5일 양천구 목동 서울식약청에서 기자회견을 열고 "인보사 관련 허가 및 사후관리에 철저히 하지 못해 국민께 혼란과 심려를 끼친 점에 죄송하다"며 "환자 안전 대책 수립과 재발 방지를 위해 최선을 다하겠다"고 밝혔다.
이 처장은 "식약처와 산하기관인 한국의약품안전관리원이 장기추적 조사를 주도적으로 이끌어 가되 비용 부담 등의 문제는 코오롱이 맡게 될 것"이라고 말했다.
이에 따라 식약처는 15년간 인보사 투여한 환자(438개 병원·3천707건)의 대한 등록 및 병·의원 방문을 통한 문진, 무릎 엑스레이, 혈액 및 관절강에서의 유전자 검사 등을 통해 이상 반응이 나타나는지 장기추적조사 하도록 했다. 또 코오롱생명과학과는 환자 피해가 발생했을 경우의 보상안 등을 협의하기로 했다.
환자는 등록 후 6개월 안에 1차 검진을 마치고, 매년 1회씩 10년 동안 관리를 받아야 한다. 나머지 5년은 문진 등으로 확인하기로 했다.
코오롱생명과학은 오는 14일까지 식약처에 이러한 이행방안이 포함된 장기추적조사 계획서를 제출해야 한다.
식약처는 코오롱생명과학의 장기추적조사 계획을 바탕으로 ▲ 환자 검진항목, 일정 등 구체적 이행방안 ▲ 환자 피해가 발생할 경우 의약품과의 인과관계 평가 기준 및 절차, 보상방안 등에 대해 조속히 협의할 계획이다.
식약처는 인보사 사태를 계기로 허가·심사 단계에서의 신뢰성 검증 절차도 강화하겠다는 계획안을 제시했다. 약사법 개정을 통해 업체가 허가 신청 시 허위자료를 제출하거나 고의로 사실을 은폐한 경우 처벌을 대폭 강화하기로 했다. 현행 약사법상 가장 높은 수준의 처벌인 5년 이하 징역 또는 5천만원 이하 벌금을 적용할 예정이다.
식약처와 코오롱생명과학 모두 인보사 사태에 책임이 있는 만큼 독립적인 별도 기관이 담당해야 한다는 시민단체들의 주장과 관련해 식약처는 반대입장을 분명히 했다.
강석연 바이오생약국장은 "의약품 부작용 보고 및 관리 등과 관련해 가장 많은 정보와 권한을 가진 의약품안전관리원에서 (이번 조사를) 담당하는 게 바람직하다고 판단했다"며 "환자 검사와 관리 등은 코오롱이 직접 하는 게 아니라 중간에 CRO(임상시험수탁기관)을 두고 수행하게 할 것"이라고 밝혔다.